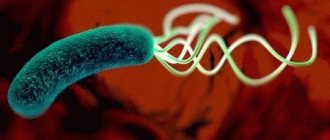
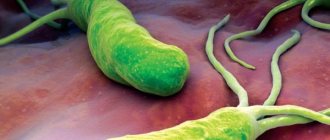
Большинство людей, страдающих язвой или гастритом, являются носителями уникальной и очень опасной бактерии — Хеликобактер пилори (Helicobacter pylori). Этот микроорганизм способен вызвать серьезные нарушения функционирования органов желудочно-кишечного тракта. Однако при лечении Хеликобактер пилори антибиотиками, назначенными лечащим врачом, можно легко избавиться от инфекции.
Бактерия Хеликобактер пилори наносит серьезный вред организму, если не пытаться от нее избавиться и не принимать профилактических мер. Сегодня с этим микроорганизмом успешно помогают бороться и медикаментозные средства.
В чем опасность
Итак, почему стоит бороться с хеликобактериозом:
- Ученые доказали связь между жизнедеятельностью патогенного микроорганизма в ЖКТ и язвой двенадцатиперстной кишки и желудка.
- Проведены исследования, которые показали, что инфекция причастна к развитию злокачественных образований слизистой.
Желудок может давать знать о присутствии бактерии Хеликобактер болью, которая вызывается повышенной секрецией соляной кислоты. В некоторых случаях процесс может протекать и бессимпто.
Лечение Хеликобактер Пилори без антибиотиков: возможно ли?
Исследования показали, что лечение хеликобактер без антибиотиков не даст положительного эффекта. Качественное лечение состоит из трех этапов. Первый ряд схемы приносит пользу. Но если этот метод не эффективен, врачи назначают следующий ряд препаратов. Когда и этот вариант не справился с инфекцией полностью, используются лекарства третьей линии. Схема лечения без антибиотиков не сможет полностью справиться с бактериями. В некоторых случаях приходится подключать четвертый компонент, который оказывает противовоспалительное действие. Хотя они назначаются на втором этапе, все же состав препарата влияет положительно на стенки органа, образовывая защитную пленку. После этого боль утихает, снимается воспаление. Но, кроме этого необходимо не только принимать таблетки, но и вести здоровый образ жизни, правильно питаться.
Формы
Существуют 2 типа хеликобактериоза:
- Скрытая форма.Зачастую пациент не подозревает наличие инфекции, поскольку нет никаких признаков. Человек в этом случае является носителем инфекции. При создании благоприятных условий бактерии начинают активно размножаться.
- Бактерия может быть виновником гастрита или язвы, острая стадия которых в дальнейшем переходит в хроническую. Кстати, именно укоренившееся заболевание является одним из основных симптомов хеликобактериоза.
Даже при отсутствии признаков, Хеликобактер пилори наносит вред состоянию и функционированию органов желудочно-кишечного тракта.
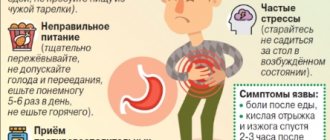
Симптомы
Обычно патогенная бактерия достаточно ярко заявляет о себе:
- Болями, локализованными в разных отделах живота, в том числе за грудиной. Болевые ощущения возникают в любое время суток. Связь появления боли с приемом пищи зависит от локализации дефекта слизистой оболочки. При язве боли появляются на голодный желудок, а после еды проходят.
- Частой отрыжкой (при этом больной ощущает кислый привкус и запах тухлых яиц изо рта).
- Метеоризмом, проблемами со стулом. При хеликобактерной инфекции наблюдаются запоры до 48 часов и регулярные расстройства желудка.
- Примесями крови и слизи в кале и рвотных массах (что свидетельствует уже о развитии осложнений).
- Тошнотой, рвотой, ощущением давления в подложечной зоне.
- Отсутствием аппетита и снижением веса без видимых причин.
- В отдельных случаях на наличие хеликобактерной инфекции могут указывать розовые прыщи на лице.
Вышеперечисленные симптомы могут указывать на разные серьезные заболевания, поэтому при наличии таких признаком следует как можно скорее обратиться к врачу и провести диагностику.
Как вылечить желудок ?
Вот такая постановка вопроса на самом деле правильная. Какая нам разница, кого там, в желудке, нужно персонально «зачистить»? Хеликобактер, стафилококк, стрептококк или еще что?
Нам нужно, чтобы не болело, чтобы кушать спокойно.
Поэтому первый шаг к исцелению это
Фитотерапия
Никто не знает, как и почему, но лечебные травы убивают только патогенных бактерий. Полезных не трогают.
Еще желательно, чтобы травы были подобраны правильно. То есть усиливали друг друга, снимали какие-то побочные эффекты друг у друга (если вдруг таковые есть).
Можно пить ромашку, можно календулу, но существенно лучше и быстрее снимают проблему правильные фитосборы. Лучший рецепт, который мне попался, оказался от к.м.н., врача-фитотерапевта с 30 летним стажем, Сергея Валерьевича Корепанова.
В конце концов я просто закупил у него партию этого фитосбора для всех, кто ко мне обращается.
Это Фитол-7. Именно желудочно-кишечный. Собран и запакетирован на предприятии АЛФИТ.
Пить его нужно, как указано в инструкции. Курсами. Курс 1 месяц.
Обычно для того, чтобы вылечиться или сильно улучшить самочувствие хватает 2-3 курса.
Заодно снимает проблемы с кишечником – журчание, запоры, поносы, дискомфорт, метеоризм, рези.
Одна упаковка как раз на месяц.
Начните с ФИТОЛа-7. КупИте, где вам быстрее или удобнее. Может, есть в вашем городе, в ближайшей аптеке. Можете купить прямо в «Алфите».
Если хотите сказать мне за опыт и советы спасибо, то просто купИте у меня тут…
Цена везде примерно одинаковая.
Второй шаг к исцелению –
Еда
Специально не пишу слово «диета» так как мой способ не про то.
Жестко себя ограничивать не нужно и нельзя. Только хуже будет.
Правила простые:
1. Едим только то, что хотим, но
2. Едим то, те продукты, те блюда, после которых НЕ появляется тяжесть или боли в желудке.
Это может быть и жареное (как ни странно и что бы ни писали в умных медицинских книжках), и вАреное, и пАреное.
Например, сплошь и рядом, везде талдычат, что овсяные каши, кисели – панацея и манна небесная. А мне вот «не шло» это и всё тут. У всех свой набор ферментов. Подбирайте продукты именно под себя.
Со временем, когда пойдет выздоровление, продуктов, после которых «не очень», будет становиться всё меньше.
3. Не переедайте. Просто следите, сколько едите. Как следить и от чего отталкиваться? А вы не знаете сколько вы обычно едите? Конечно знаете. Не с закрытыми глазами ведь за столом. Уменьшайте на четверть. Прекращайте есть до наступления чувства сытости.
Ну, вы поняли – не четверть оставляете себе, а порцию уменьшаете на четверть. Съедаете ¾ от обычной своей порции.
4. Не пейте сразу после еды. Можно запивать по чуть. Так чтобы в желудок шла такая полужидкая субстанция. Или, если уж очень хочется после еды попить чай, то пейте в хорошую прикуску. То есть так, чтобы в желудок не одна только жидкость лилась, а такая полужидкая субстанция. Делайте так. Результат почувствуете сразу.
5. Как можно меньше сладкого. Может показаться, что противоречит пункту 1, но что сделаешь. Это очень важно. Так называемых быстрых углеводов как можно меньше. Желательно около нуля. Это сахар, газировки, печенья, пирожные, торты, булочки и хлеб из муки высшего сорта, белый рис, манка. Заменяйте быстрые углеводы медленными.
Как проводится диагностика
При подозрении на наличие бактерии Хеликобактер пилори необходимо провести обследования:
- Анализ кала на антиген Helicobacter Pylori. В большинстве случаев лаборанты обнаруживают в кале частички бактерий, что и дает все основания полагать, что их колонии заселяют желудочно-кишечный тракт.
- Анализ крови на антитела. Этот метод диагностики нельзя назвать точным на все 100%. Дело в том, что даже после перенесения хеликобактерной инфекции антитела имеют свойство сохраняться в течение длительного периода времени.
- Одним из лучших способов диагностики считается дыхательный тест. Его преимущества заключаются в высокой точности и бюджетности. Однако необходимо помнить, что при несоблюдении правил подготовки можно получить ложный результат. Для повышения надежности за полмесяца до проведения диагностики нужно отказаться от употребления антибиотиков, противовоспалительных и ряда других препаратов. А за 3 дня до процедуры избегайте приема алкогольных напитков и курения. За сутки перестаньте пить кофеиносодержащие и газированные жидкости.
- Часто при язве желудка и подозрении на другое заболевание кишечного тракта назначают эндоскопическое обследование. В процессе него берется биопсия — небольшой образец слизистой. Такая диагностическая манипуляция является одной из самых высокоинформативных
Отзывы врачей и их пациентов, страдающих инфекцией, говорят о том, что не стоит надеяться на результаты одного метода диагностики. Чтобы подстраховаться, специалисты назначают сразу несколько обследований.
Хеликобактерная инфекция у детей: проблема, анализ обобщенных данных
Хронические воспалительные заболевания верхних отделов пищеварительного тракта чрезвычайно распространены в современном мире. По данным крупномасштабных эпидемиологических исследований за последнее десятилетие их показатель вырос на 37% и колеблется от 100 до 550 на 1000 детей [20]. В детской популяции в структуре этих заболеваний хронический гастродуоденит имеет стабильно высокий уровень — в пределах от 153 до 235‰.
Анализ клинико-анамнестических данных больных, проживающих на территории Московской области, позволил выявить кардинальные особенности клинической симптоматики хронического гастродуоденита у детей [20]. К ним относились: преобладание тяжелых вариантов болезни с частыми, затяжными обострениями и выраженной сезонной зависимостью их возникновения, с отчетливым нарастанием распространенности заболевания у девочек, в раннем и дошкольном возрасте.
Используемая современная методология количественной оценки факторов риска (относительный, атрибутивный риск) дала возможность авторам доказать, что хронический гастродуоденит развивается под влиянием комплекса экопатологических, биологических и социальных факторов, что подтверждает актуальность разработки специальной программы медико-экологической реабилитации [20].
Несмотря на интенсивный научный поиск и значительный прогресс в области эпидемиологии, морфологии, иммунологии, микробиологии и других специальностей, единая патогенетическая концепция гастродуоденита не разработана. Однако проясняется патофизиологическая сложность заболевания. Не вызывает сомнения, что факт признания Нelicobacter pylori этиологическим агентом большинства гастродуоденальных заболеваний и разработка эффективных схем антибактериального уничтожения возбудителя является важнейшим достижением в современной клинической гастроэнтерологии. Практический опыт подтвердил, что морфологические изменения, возникающие в слизистой оболочке гастродуоденальной зоны, подвергаются обратному развитию в случае своевременно проведенной эрадикации Н. pylori [1, 2, 9].
Наиболее убедительно доказана роль Н. pylori в этиологии язвенной болезни желудка и двенадцатиперстной кишки. Риск ее развития в течение жизни у инфицированных людей варьирует от 3% в США до 25% в Японии [4]. Эрадикация H. pylori — это утвержденный способ первоначальной терапии язвенной болезни желудка и двенадцатиперстной кишки. Более того, в проспективном продолжительном исследовании, включающем около 400 пациентов с язвенными кровотечениями, было установлено, что их рецидивы после эрадикации H. pylori не развиваются. Если эрадикация была эффективной, то назначение поддерживающей антисекреторной терапии не является обязательным [18].
На основании недавно полученных данных считают, что хеликобактерная инфекция повышает риск развития рака желудка [5, 6]. Кроме того, хеликобактерная инфекция повышает риск развития MALT лимфомы желудка. Эрадикационная терапия в настоящее время является стандартным подходом к лечению больных с I стадией опухоли и вызывает ремиссию примерно у 70% больных [5].
Накапливаются данные, демонстрирующие ассоциацию между хеликобактерной инфекцией и идиопатической тромбоцитопенией. Частота хеликобактериоза у больных с идиопатической тромбоцитопенией составляет 58%. Проведенное метааналитическое сравнение, включающее 16 исследований с проспективным когортным дизайном и одно рандомизированное исследование, показало строгую корреляцию между эрадикацией H. pylori и увеличением числа тромбоцитов [17]. Эрадикационная терапия позволяет добиться полного или частичного восстановления числа тромбоцитов примерно в половине случаев. Причиной этого факта может быть сходство антигенов тромбоцитов и H. pylori. Нельзя исключить, что H. pylori-инфекция может способствовать развитию железодефицитной и мегалобластной анемии. Недавно в клиническом исследовании было продемонстрировано нарушение всасывания железа у инфицированных пациентов и его восстановление после эрадикации микроорганизма [7].
Многие детали процесса колонизации слизистой оболочки Н. pylori до конца не изучены, однако механизмы его схематично можно представить следующим образом: хемотаксис по направлению к слизистой оболочке желудка — проникновение бактерии в слизь — адгезия к рецепторам слизи и слоям, связанным с ней, — адгезия к эпителиальным клеткам — размножение ассоциированных со слизистой оболочкой бактерий.
Н. pylori, длительно персистируя в слизистой оболочке желудка, вызывает ряд патохимических изменений и постоянную антигенную стимуляцию. Антигенспецифические и антигеннеспецифические реакции иммунной системы при инфицировании Н. рylori могут контролировать развитие инфекции, но могут также быть причастны к развитию повреждения слизистой оболочки желудка. В этой ситуации происходит реорганизация цитоскелета эпителиоцитов и ряд других изменений: эпителиальные клетки отвечают на это продукцией цитокинов — интерлейкина-8 и некоторых других хемокинов. Эти цитокины также приводят к миграции лейкоцитов из кровеносных сосудов, развивается активная стадия воспаления. Активированные макрофаги секретируют гамма-интерферон и фактор некроза опухоли. Последние сенситизируют рецепторы лимфоидных, эпителиальных и эндотелиальных клеток, что в свою очередь привлекает в слизистую оболочку новую волну клеток, участвующих в иммунных и воспалительных реакциях. Каталаза и супероксиддисмутаза, продуцируемые Н. рylori, нейтрализуют фагоциты, позволяют микробу избежать фагоцитоза и способствуют гибели полиморфноядерных лейкоцитов. Метаболиты активного кислорода нейтрофилов оказывают повреждающее действие на эпителиоциты желудка. Создаваемый порочный круг влияет на структуру эпителия и формирует хронический патологический процесс в слизистой оболочке, что в дальнейшем приводит к нарушению нормальной физиологической регенерации железистого эпителия. Доказано, что микроорганизм обусловливает дисрегенераторные процессы: влияет на пролиферацию и на апоптоз эпителиоцитов слизистой оболочки желудка. По современным представлениям, классический антрум-гастрит с мононуклеарной инфильтрацией собственной пластинки слизистой оболочки желудка является следствием взаимодействия грамотрицательных бактерий с организмом хозяина. На сегодняшний день утверждается точка зрения, согласно которой характер воспалительного ответа, его интенсивность и опосредованные им отдаленные эффекты (атрофия, гипохлоргидрия, развитие дистального рака желудка) определяются генотипом хозяина. Установлено, что худший прогноз можно ожидать у гомозигот IL-1В-31 Т/Т.
Рассматривая механизмы развития патофизиологических реакций при возникновении ассоциированных с Н. рylori заболеваний, необходимо оценить роль и место пилорического хеликобактера в целостной симбионтной эндоэкосистеме организма. На безусловную значимость состояния микробной экологии пищеварительного тракта для колонизации желудка Н. рylori и развития связанного с этими бактериями патологического процесса указывают наблюдения японских исследователей, показавших, что оральное инфицирование безмикробных крыс Н. рylori никогда не сопровождалось колонизацией слизистой оболочки желудка животных и возникновением у них гистологических изменений. Демонстративными являются собственные данные (2001), согласно которым в изучаемом микробиотопе — толстой кишке отмечалось снижение и изменение свойств индигенной микрофлоры, модификация общей микробной обсемененности и появление условно-патогенных микроорганизмов, несвойственных данному биотопу, сдвиг микробных сообществ в сторону ассоциативного роста грамотрицательных бактерий (являющихся более стойкими к антибактериальному действию окружающей среды и проявляющих более выраженную, по сравнению с грамположительными, склонность к паразитизму). В микробиоте толстой кишки частота низких титров бифидобактерий (71,4%) преобладала над показателями численности популяции лактобактерий (55,2%), больше высевалось клебсиелл и грибов рода Candida. Полученные результаты нарушения микробной колонизации исследуемого микробиотопа дали нам основание отнести дисбактериоз к биомаркерам снижения общей колонизационной резистентности пищеварительного тракта.
Хеликобактериоз является наиболее распространенной хронической бактериальной инфекцией у человека и имеет как этнографическую (характеризующую расу), так и социально-экономическую детерминацию. На сегодняшний день доказано, что инфицирование Н. pylori в различных регионах России имеет весьма широкий диапазон вариации и составляет от 72% до 95%. Результаты современных эпидемиологических исследований в Сибири свидетельствуют о том, что заражение Н. pylori начинается в раннем детском возрасте, достигая 33,3% к 10 годам и 56,3% — к 17-летнему возрасту, что полностью согласуется с данными, полученными в других территориях России и странах ближнего зарубежья: в Санкт-Петербурге 48% обследованных в возрасте 15–19 лет были инфицированы, в Эстонии 60% детей в возрасте 15 лет оказались серопозитивными. Обращает на себя внимание и тот факт, что частота выявления Н. pylori среди российских подростков существенно выше, чем в развитых странах. Например, доля серопозитивных детей в возрасте 10–15 лет варьировалась от 6,6% в Новой Зеландии, 11% в Великобритании, 13,4% в Италии, 16,1% в Швеции, до 17,9% в США. Что касается развивающихся стран, то инфекция Н. pylori встречается в Албании у 96%, Индии — 84%, Китае — 67%, Чехии — 63%, Мексике — 55,3% подростков. Используемая современная методология комплексной оценки факторов риска дала возможность определить ассоциацию Н. pylori с социально-экономическими условиями, прежде всего — с проживанием в неблагоустроенном жилье, низким уровнем образования и физическим трудом родителей, низким качеством питания. Безусловно, для повседневной практики важен установленный факт, что основным источником заражения служат непосредственные контакты детей с инфицированными лицами, и, как свидетельствуют исследования, проведенные в последние годы, этим источником обычно являются члены семей.
Есть данные о том, что заражение детей происходит от своих родителей. С помощью серологических исследований Н. pylori, проведенных среди населения Туркменистана (2003), установлено, что сразу после рождения у значительной части детей (49%) имелись антитела к Н. pylori, к году — их доля снижалась почти в 2 раза (26%), а затем постепенно увеличивалась в каждой возрастной группе: к 5 годам — 46%, к 10 годам — 53%, к 14 — 82%.
При изучении распространенности Н. pylori-ассоциированных болезней в детском возрасте установлена зависимость инфицирования от давности хронического гастрита, например, у больных с кратким анамнезом заболевания Н. pylori выявляется в 15% случаев, тогда как при продолжительности болезни более 5 лет возбудитель обнаруживается в 70%. Исследования, проведенные в Китае, США, Финляндии, показали, что ежегодное увеличение заболеваемости Н. pylori-ассоциированных гастритов составляет приблизительно 1%.
Поперечные клинико-эпидемиологические исследования, проведенные в России на территориях с разным уровнем антропогенного загрязнения, также подтверждают высокую распространенность Н. pylori-позитивного хронического антрального гастрита у детей, однако этот показатель чрезвычайно разнообразен и составляет от 53% до 90%.
Многочисленные публикации свидетельствуют о том, что инфекция Н. pylori является причиной всех наиболее тяжелых форм гастродуоденальной патологии у детей. Наиболее часто Н. pylori обнаруживается при эрозивном (86%) и гипертрофическом (82%) гастритах, несколько реже при других формах гастрита: субатрофическом (60%), атрофическом (58%) и поверхностном (49%). При язвенной болезни двенадцатиперстной кишки Н. pylori выделяют чаще (91–100%), чем при язвенной болезни желудка (70–100%).
Таким образом, инфекция Н. pylori имеет глобальное значение и широко распространена среди детской популяции во всем мире. Большинство исследователей соглашается с тем, что Н. pylori-инфекция обычно приобретается в детском возрасте.
Существенный прогресс был достигнут в разработках схем лечения инфекции Н. рylori, ряд из которых является общепризнанным и рекомендуется на национальном и европейском уровнях. При назначении терапии мы руководствуемся международными рекомендациями по лечению Н. pylori-ассоциированной гастродуоденальной патологии (Маастрихт-3, 2006), согласно которым общий курс лечения должен быть увеличен до 10 или 14 дней. Тем не менее, применение 7-дневных схем возможно и показано при доказанной их эффективности в конкретном регионе. В Московской области в течение последних 15 лет антихеликобактерная тройная семидневная терапия (Де-Нол + Амоксициллин + Фуразолидон), имеющая 86% эффективности, остается одной из наиболее широко использующихся в практике врача-педиатра.
Как было указано выше, инфекция Н. рylori, воздействуя на организм, приводит к нарушению баланса микрофлоры толстой кишки, который усугубляется после перорального приема антибиотиков. Полученные к настоящему моменту данные свидетельствуют о том, что после антихеликобактерной терапии у всех больных наблюдается нарушение микробиоценоза кишечника, а клинические признаки дисбактериоза выявляются у 45,5% больных. Так, по нашим данным, при исследовании кала на дисбактериоз у больных с Н. pylori-ассоциированным гастритом, получающих комбинированную терапию, отмечался дефицит нормальной микрофлоры толстой кишки, сочетающийся с ростом условно-патогенных микроорганизмов, в том числе грибов рода Candida [19]. Последнее исследование, проведенное Е. В. Каннер [3], подтвердило положение о том, что обострение хронического гастродуоденита, ассоциированного с Н. pylori-инфекцией, сопровождается грубыми нарушениями в составе нормофлоры толстой кишки у детей. При изучении метаболитного статуса копрофильтратов установлено снижение относительного содержания уксусной кислоты, повышение доли пропионовой и масляной, изменение анаэробных индексов и отношений изомеров кислот к отношению неразветвленных кислот. Было установлено, что проведение стандартной антихеликобактерной терапии усугубляет микроэкологический дисбаланс в кишечнике у 57,1% больных. Очень важный практический аспект работы касается целесообразности профилактического назначения пре- и пробиотиков, энтеросорбентов с доказанным цитомукопротективным эффектом с первых дней начала эрадикационной антихеликобактерной терапии, что снижает риск развития антибиотико-ассоциированной диареи в 10 раз [3].
Многие вопросы относительно того, нужно ли детям назначать пробиотики на фоне антибиотикотерапии, остаются без ответа. Результаты проведенного метаанализа свидетельствуют об умеренных преимуществах приема отдельного пробиотического штамма, например, Saccharomyces boulardii, или Lactobacillus GG, или комбинации пробиотиков (например, Bifidobaterium lactis и Streptococcus thermophilus) для профилактики антибиотико-ассоциированной диареи [10, 11, 12]. В настоящее время нет объективных данных об эффективности назначения других пробиотических штаммов детям.
Saccharomyces boulardii — непатогенные пробиотические дрожжевые грибы, изначально изолированные из плодов личи, произрастающего в Индонезии, и впервые примененные для лечения диареи во Франции в начале 1950 гг. Лиофилизированная форма находит широкое клиническое применение в Европе, Азии, Африке, Центральной и Южной Америке. Доклинические и экспериментальные исследования продемонстрировали противовоспалительную, антибактериальную, ферментативную, метаболическую и антитоксическую активность препарата. Saccharomyces boulardii обладают естественной резистентностью к антибиотикам и кислотности желудочного сока, что очень важно. Эффективность Saccharomyces boulardii обусловлена прямым блокирующим действием на рост патогенных штаммов. Секретируя протеазу (54 кДа), пробиотик нейтрализует определенные бактериальные токсины, другие ферментные действия осуществляются выделением полиаминов, в результате чего увеличивается количество дисахаридов (лактазы, сахарозы, мальтазы, аминопептидазы), вырабатываемых щеточной каемкой микроворсинок. Увеличение секреции полиаминов стимулирует созревание энтероцитов и способствует достижению максимальной абсорбции глюкозы на их мембраны. В недавнем рандомизированном двойном слепом плацебо-контролируемом исследовании была показана эффективность Saccharomyces boulardii у детей с острым гастроэнтеритом и взаимосвязь пробиотика с иммунным ответом организма [12]. Значительное достоверное увеличение уровня CD8 в группе детей, получавших Saccharomyces boulardii, свидетельствует о провоспалительной активности пробиотика, приводящей к высвобождению цитокинов и активации CD8 клеток, что, по-видимому, помогает ограничить инфекционный процесс. Это исследование согласуется с результатами других авторов, согласно данным которых выявлено незначительное повышение TGF-бета и снижение TNF-альфа (по механизму обратной отрицательной связи провоспалительные цитокины, стимулированные CD8, влияют на уровень TNF-альфа). Иммунологические изменения обнаружены в отношении сывороточного IgA и СРБ (С-реактивный белок). Значительное достоверное повышение уровня первого показателя и снижение второго по сравнению с исходными значениями также подтверждает важную способность пробиотика уменьшать воспалительный процесс.
Согласно опубликованным данным, Saccharomyces boulardii эффективен в качестве профилактического и лечебного средства при диарее, вызванной приемом антибиотиков, Clostridium difficile, хронической диарее, обусловленной лямблиозом, амебиазом, «диарее путешественников», у пациентов с диареей, находящихся на парентеральном питании, с ВИЧ-инфекцией. Однако основным показанием к использованию препарата является острая диарея у детей и взрослых. Много сообщений ясно показывают, что пробиотик Saccharomyces boulardii снижает продолжительность диареи (нормализация консистенции и частоты стула) и время пребывания больного в стационаре примерно на 24 часа [13, 14, 15, 16].
Многосторонний механизм действия и эффективность применения Энтерола® 250 по отношению к Бифидумбактерину в комплексной терапии хеликобактер-ассоциированных гастродуоденитов у детей были продемонстрированы в нашем исследовании [19]. Больные были рандомизированы на 2 группы: 1 группа (n = 23) — получала схему Де-Нол (240 мг), Флемоксин Солютаб (1000 мг), Фуразолидон 200 мг, Энтерол® 250 мг 2 раза в день 7 дней и далее Де-Нол 2 недели и Энтерол® 3 недели: 2 группа (n = 36) — Фуразолидона 7 дней, далее Де-Нол и коммерческие штаммы Бифидумбактерина 10 доз 3 раза в день 4 недели. Непосредственные результаты лечения оценивались по совокупности клинических, лабораторных и инструментальных данных. Лечение оказалось успешным в первой группе детей, применение Энтерола® существенным образом сказалось на быстрой стабилизации состояния больных и исчезновении гастроинтестинальных проявлений дисбактериоза. Отчетливый элиминационный эффект пробиотика получен в отношении клебсиелл, цитробактера, гемолизирующих штаммов эшерихий, грибов рода Candida, что сопровождалось в свою очередь нормализацией количественного содержания бифидобактерий, лактобацилл, кишечной палочки и энтерококков. Отмечалась хорошая динамика в копрограммах: снижалось количество непереваренных мышечных волокон, растительной клетчатки и зерен крахмала, ликвидировалась йодофильная флора. Были получены следующие доказательства преимущества комплексной терапии с Энтеролом® 250. Данный пробиотик, назначенный больному с первого дня приема антихеликобактерных средств, позволяет «защитить» индигенную микрофлору, снизить риск развития более тяжелых дисбактериозов, провоцируемых ятрогенным вмешательством используемых антимикробных препаратов, и существенно влиять на эффективность тройной терапии с базисным препаратом висмута (показатель эрадикации по протоколу составил в 1 группе — 91,3%, соответственно во 2 группе — 83,3%).
Таким образом, высокая терапевтическая эффективность, превосходные фармакологические свойства, возможность использования вместе с другими лекарствами, высокий профиль безопасности, удобный режим приема делают Энтерол® препаратом выбора для профилактики и коррекции дисбиотических нарушений, ухудшающих течение гастроэнтерологических заболеваний у детей.
В заключение хотелось бы представить разработанную нами многоуровневую программу лечения детей с Н. pylori-ассоциированными заболеваниями. Первый уровень — тщательный анализ клинической симптоматики обострения хронической гастродуоденальной патологии. Второй уровень — первичная диагностика Н. pylori-инфекции: фиброгастродуоденоскопия (ФГДС) + биопсия (уреазный «хелпил-тест» + гистологическое исследование). Мероприятия третьего уровня (7 дней) — эрадикация Н. pylori-инфекции: Де-Нол + Амоксициллин + Фуразолидон + Энтерол®. Мероприятия четвертого уровня (3–5 недель) — восстановление морфофункционального состояния слизистой оболочки желудка и двенадцатиперстной кишки с помощью Де-Нола.
По вопросам литературы обращайтесь в редакцию.
Н. И. Урсова, доктор медицинских наук, профессор
МОНИКИ им. М. Ф. Владимирского, Москва
Начало лечения
Прежде чем врач подберет схему терапии, он обязан назначить тест, определяющий чувствительность бактерии к антибактериальным средствам. Это поможет выбрать правильные препараты, убивающие бактерию.
Принципы эффективного лечения антибиотиками при Хеликобактер пилори:
- Изначально следует пройти обследования, позволяющие выявить бактерию в органах желудочно-кишечного тракта.
- Желательно, чтобы терапию H. Pylori прошли не только больные, но и их близкие и родственники, проживающие вместе с пациентом. При этом желательно обследовать домочадцев.
- После проведения медикаментозной терапии проводится контрольную диагностику. Если вновь обнаружен патогенный микроорганизм, то рекомендуется повторный прием антибиотиков в течение 7-14 и более дней. При этом вероятна замена предыдущих антибактериальных средств на новые. Длительность курса устанавливает врач.
- На сегодняшний день наиболее эффективным является прием сразу трех и даже четырех препаратов.
Если медикаментозная терапия не работает, Хеликобактер можно попробовать вылечить другим способом. Американские ученые провели эксперимент на 18 пациентах, в ходе которого удалось выяснить, что виновник многих заболеваний желудочно-кишечного тракта уязвим к свету. Фототерапия показала высокую эффективность. Тем не менее еще необходимо провести ряд дополнительных исследований. После них станет понятно, возможно ли заменить терапию антибактериальными средствами на лазер.
Антибактериальная терапия
В основном антибиотики принимаются при гастрите и наличии H. Pylori в ЖКТ.
Однако есть и другие показания:
- язва желудка или двенадцатиперстной кишки;
- мальтома и резекция желудка;
- опухоли ЖКТ;
- нехватка в организме железа;
- развитие анемии.
Как бы странно это не звучало, но не во всех случаях проводится медикаментозная терапия. Она необходима только в случае, если есть риск развития язвы или же имеются неспецифические симптомы.
Принцип выбора антибиотиков
Для лечения инфекции назначаются одновременно несколько препаратов. Существуют разные линии медикаментозных средств против Хеликобактер пилори.
Их выбор зависит от таких факторов:
- Возраст пациента с H. Pylori.
- Реакция организма на антибиотики (для этого обязательно необходимо провести тест на чувствительность к лекарствам).
- Противопоказания к приему определенных групп медикаментов. Например, некоторые нельзя принимать при почечной недостаточности.
Так же врач должен подбирать средство, учитывая:
- Его способность убивать колонии бактерий в условиях кислой среды, созданной воздействием соляной кислоты.
- Биодоступность антибиотика — она должна быть высокой.
- Минимальное количество побочных явлений (особенно это важно для терапии детей и беременных женщин).
Антибиотики при хеликобактерной инфекции следует принимать только по назначению врача и под его контролем. После завершения куса терапии обязательно проводится повторная диагностика, позволяющая убедиться, что лечение прошло успешно.
Лечение Хеликобактер Пилори антибиотиками
Бактерия Helicobacter pylori широко распространена, известная, как опасный микроорганизм, которому не страшна соляная кислота. Она провоцирует появление гастродуоденита. Выявлено, что меры борьбы основаны на разных препаратах. Но, большинство антибактериальных лекарств не приносит большой пользы. Не все они проникают под слизистый слой, в котором находится бактерия. При запущенной болезни возможно развитие онкологии. По этой причине важно выяснить, какими антибиотиками лечить Хеликобактер.
Кларитромицин при Хеликобактер пилори
Этот препарат является 14-членным макропидом, производным эритромицина, соответствующий уровнем активности и методом использования. Но, по сравнению с эритромицином устойчивее к влиянию кислоты. Препарат с длительным периодом выведения. Существует тройная схема лечения антибиотиками.
Кларитромицин назначается взрослым – 250 мг (1 капсула) два раза в сутки. Пить таблетки от 6 до 14 дней. Если присутствует тяжелая форма заболевания, доза увеличивается до 2 капсул два раза на день. Запивать водой, глотать лекарство независимо от приема еды.
Азитромицин при Хеликобактер пилори
Препарат имеет большой спектр действия, действует бактериостатически. Он снижает, действует угнетающе еще на стадии трансляции пептидтранслоказу, синтез белка. Также замедляет рост бактерий, не допускает их размножение, оказывает бактерицидный эффект. Действует на возбудителей как внутриклеточных, та и внеклеточных, которые вызваны чувствительными возбудителями язвенной болезни 12-перстной кишки, которая ассоциируется с Helicobacter pylori.
Принимать лекарство необходимо с осторожностью. Беременным можно только в том случае, если польза от лечения превышает риск. Не рекомендуется приписывать детям, у которых выраженные нарушения работы таких органов, как почки или печень. Глотать независимо от
Тинидазол : эффективен от Хеликобактер
Активен препарат при анаэробных бактериях, микроаэрофильных Helicobacter pylori либо смешанными аэробно-анаэробными инфекциями. Комбинируют с ним антибиотики от хеликобактер.
Не рекомендуется в первом триместре беременности. Возможно только в том случае, если без приема лекарств невозможно обойтись и положительный результат превышает риск для ребенка. Не позволяется пить лекарство детям, не достигшим 12 лет. Взрослым – 4 таблетки (500 мг) 1 раз в день. Детям – 50 мг/кг раз в сутки.
Левофлоксацин
Назначается при заболевании острым синуситом, Helicobacter pylori, инфекций, вызванных чувствительными возбудителями к к левофлоксацину. Доза определяется лечащим врачом.
Длительность терапии от недели до двух. Принимать внутрь – 250 – 750 мг раз в день до приема пищи или между ними. Раствор вводится внутривенно, медленно. В течении часа до 500 мг, а 750 мг до полутора часа.
Тетрациклин
Этот препарат останавливает биосинтез белка, объединяется необычным методом с 30‑S субъединицей рибосомы. Он доказал свое эффективное действие на H. Pylori. Сохраняется интенсивность даже при низком уровне pH. Включается лекарство в систему лечения второго ряда.
Действует как бактерицидный препарат, повышает уровень устойчивости оболочки желудка к негативному воздействию. Реконструируются функции защиты, предотвращает рецидивы заболевания. Во время приема лучше не употреблять соки, молоко. Курс лечения до двух недель. Для усиления эффекта добавляются антисекреторные таблетки. Но, такого лечения не достаточно, только комбинированное лечение позволяет добиваться излечения в 980% случаев. Поэтому составляется специальная схема лечения хеликобактера антибиотиками +с денолом.
Амоксициллин при Хеликобактер
Это антибиотик, относящийся к ряду пенициллинов, по динамичности очень подходит к ампициллину. В кислой среде ведет себя стабильно. Действует местно, а также системно. Helicobacter pylori показывает чувствительность к препарату, но для качественного лечения необходим комплексный подход.
Применять лекартсво 4 раза на день по 500 мг, либо 2 раза по 1000 мг. Есть в виде таблеток или суспензии, всасывается быстро и почти полностью. Прием пищи не зависит от употребления лекарства.
Метронидазол
Хеликобактер чувствительна к препарату. После применения в желудочной кислоте образуется высокая концентрация лекарства. Это позволяет достичь хорошего терапевтического эффекта. В процессе обмена веществ «метронидазол» проходит активацию нитроредуктазой, что приводит к устранению структуры ДНК бактерии, после чего они погибает. Растворяется быстро и хорошо, примерно за 1 час.
Период выведения равен 8 – 10 часам. Принимать взрослым по 2 таблетки на сутки (500 мг). Детям назначается препарат в зависимости от массы тела (30 мг за 3 приема).
Рифамбутин
Антибиотик активен, располагается как внутри, так и снаружи клеток. Применяется как для лечения, так и профилактики болезней ЖКТ, при эрадикации бактерии Helicobacter pylori Часто рекомендуется лекарство при неэффективности схем первой и второй линии.
Применяется не зависит от приема пищи. Для взрослых 2 капсулы (300 мг) раз в сутки. После приема хорошо всасывается. Равномерно распределяется в других органах, тканях, накапливается в значительной концентрации внутриклеточно.
Перечень препаратов, необходимых для терапии
Список лекарственных средств включает несколько групп:
- Медикаментозная терапия подразумевает назначение препаратов висмута (например, Де-нол). Однако имеются схемы лечения, когда обходятся и без этих лекарств.
- Непосредственно сами антибиотики. Чаще всего отечественные врачи назначают: Аугментин, Флемоксин, Клацид, Ормакс. Возможно комбинированное лечение двумя и более видами антибиотиков (обычно если не назначаются препараты висмута).
- Антисекреторные лекарства: Ранитидин, Омез, Лансопразол, Гастроцепин и другие.
- Противомикробные медикаменты (в случае необходимости) — например, Макмирор.
- Ферментные препараты (Мезим, Пангрол, Креон) назначаются для улучшения пищеварения и снятия чрезмерной нагрузки с поджелудочной железы. Чаще всего без них не обходится лечение заболеваний ЖКТ, сопровождаемых наличием хеликобактерной инфекции.
- Антибиотикотерапию обязательно сопровождает прием лакто- и бифидобактерий (Бифиформ, Линекс, Ацепол) для нормализации работы кишечника и (или) средства для предотвращения возникновения кандидоза (Флуконазол, Нистатин, Пимафуцин и др.).
В большинстве случаев нельзя прогнозировать результат медикаментозной терапии. Объясняется это устойчивостью бактерии к лекарствам. Ведь многие люди бесконтрольно принимают антибиотики для терапии всевозможных болезней. Однако при назначении комбинированной терапии результат в большинстве случаев положительный. В сложных ситуациях есть возможность сдать анализы на выявление чувствительности бактерии H. Pylori к определенным антибактериальным средствам.
На данный момент не существует прививки от Хеликобактер пилори. Тем не менее несколькими годами раннее лучшие ученые мира принялись за разработку вакцины. Специалисты хотели добиться того, чтобы препарат можно было употреблять во время приема пищи. Однако выявить средство, которое было бы эффективно в условиях кислой среды, оказалось проблематично.
Пример схемы лечения
Так как наиболеераспространенные схемы антибиотикотерапии хеликобактериоза включают прием двух основных медикиментов, врач, вероятнее всего, предложит вам прием препарата Де-нол в совокупности с другим предпочитаемым им антибиотиком или схему Кламокс+Кларицин.
Точные виды препаратов, подходящие именно вам, дозировку и длительность лечения может рекомендовать только ваш лечащий врач. Не занимайтесь самолечением!
Препараты висмута
Эта схема лечения Хеликобактер пилори антибиотиками применяется чаще всего. Врач назначает один антибактериальный препарат и дополняющее его средство.
Кларитромицин или Тетрациклин. Оба лекарства необходимо принимать дважды в день. Средняя дозировка для взрослого человека составляет 0.5 г. Также принимается ингибитор протонной помпы или блокатор гистаминовых рецепторов (Циметидин или Роксатидин). Точную дозировку назначает лечащий врач.
Антибиотикотерапия
Обычно назначается один вид (Амоксициллин, Тетрациклин и др.) и два дополнительных препарата (Фамотидин, Квамател или Ранитидин). Курс антибактериальных медикаментов по данной схеме длится не менее 10 дней.
При этом специалист вправе увеличить дозировку средств и изменить двухразовый прием на четырехразовый.
Дополнительные медикаменты
Разбирая третью схему лечения H. Pylori антибиотиками, стоит отметить, что она комбинированная. То есть подразумевает одновременный прием двух антибактериальных и двух дополнительных препаратов. Помимо этого, используются ингибиторы протонной помпы и блокаторы гистаминовых рецепторов.
Так же специалист может назначить Вентер или Мизопростол. Эти лекарства защищают стенки желудка от агрессивного воздействия соляной кислоты.
В период лечения Хеликобактер врач назначает витамины и пребиотики. Ведь давно известно, что препараты антибактериального действия убивают как патогенные микроорганизмы, так и полезные.
Возможные побочные эффекты
Примерно у 15-20% пациентов при терапии H. Pylori антибиотиками возникают побочные явления.
К числу основных относятся:
- боль в животе;
- кашель;
- диарея;
- металлический привкус во рту;
- аллергическая реакция;
- тошнота и рвотные позывы;
- головная боль и головокружение;
- светочувствительность;
- у женщин могут появиться выделения из влагалища.
В 5% случаев наблюдаются такие негативные последствия, как: гепатит, облысение, нарушения сердечного ритма, токсическое поражение ЦНС.
Как диагностировать заболевание?
Первый шаг к составлению программы является обследование. Проводится оно в первую очередь для людей с повышенным риском. Существуют разные варианты диагностики, основаны на уровне активности инфекции. Свойство хеликобактера заключается в расщеплении мочевины с образованием углекислого газа и аммиака, этим отличает его от других микробов. Пациент при болях в животе должен обратиться сначала к врачу гастроэнтерологу. При локализации усугубления ситуации в верхних отделах назначается фиброгастродуоденоскопия. Это основной метод обследования, позволяющий видеть изменения слизистой, включая язвенный дефект.
При прохождении данной процедуры берется биоптат. Заключается она в гистологическом исследовании, а также проведении уреазного теста, который определяет присутствие бактерии Helicobacter рylori. Если в биоптате есть инфекция, она при помощи реакции расщепления мочевины определяется благодаря бумажном индикатору. Он содержит сложный химический состав, изменяющий цвет при наличии бактерии.
Этот вариант очень удобный, практичный, результат готов через 2 – 3 минуты. Также есть дыхательный тест, применяя который можно по выдыхательному аммиаку обнаружить присутствие бактерии.
Возможно ли лечение без антибиотиков
Есть мнение, что от Хеликобактер можно избавиться и с помощью народных рецептов, натуральных сборов.
Обнаружение Хеликобактер пилори — прямое показание для назначения антибактериальной терапии. А вот для профилактики фитотерапия сама по себе очень даже эффективна.
Хеликобактер пилори — умная бактерия, которая способна выживать даже в кислой среде, где большинство других организмов погибают. Поэтому только прием настоев из арсенала народной медицины не приведет ни к чему хорошему. А некоторые из снадобий даже способны ухудшить состояние больного.
Питание при инфекции
Помимо приема антибиотиков рекомендуется придерживаться основ сбалансированного рациона и питаться по 5-6 раз в день небольшими порциями.
Специалисты советуют помнить о принципах диеты:
- Тщательно пережевывать пищу. Если это дается сложно пациенту, то рекомендуется употреблять перетертую еду.
- Ограничить применение в пищу соли (не более 2 ч. л. в день). Для контроля желательно приправлять блюдо, которое находится уже в тарелке.
- Не кушать слишком горячую или холодную пищу.
- В период лечения инфекции употреблять не менее 2 л воды в сутки.
- Избегать жирной, жареной еды.
- Не голодать. Все новомодные диеты приводят к раздражению слизистой желудка.
Чтобы добиться стойкой ремиссии, рекомендуется придерживаться данных правил питания в течение 1-1.5 года.
Профилактика заболевания
Немногим людям известно, что у человека не вырабатывается иммунитет к хеликобактерной инфекции, поэтому возможно очередное заражение.
Если вы хотите избежать повторной терапии, специалисты рекомендуют:
- Иммунитет к хеликобактерной инфекции не вырабатывается, поэтому возможно повторное заражение. Чаще всего это происходит дома. Избежать поможет использование личной посуды.
- Соблюдать правила гигиены. К мытью рук приучайте и ребенка.
- Помнить, что бактерия передается через слюну. Поэтому поцелуи с людьми, в состоянии здоровья которых вы не уверены, могут стать причиной заражения. Малышам не стоит разрешать делиться фруктами по принципу «дай откусить», а девушкам не рекомендуется пользоваться одной помадой на двоих с подругой.
- К активной жизнедеятельности микроорганизма приводит увлечение спиртным. То же относится и к курению (в том числе и пассивному).
- Приучить деток не употреблять немытые овощи и фрукты.
- Регулярно водить домашнего питомца на профилактический осмотр к ветеринару. До недавнего времени не было информации о том, что можно заразиться инфекцией от животных. Однако теперь есть все основания полагать, что кошки, собаки, обезьяны и свиньи переносят болезнетворную бактерию.
- При первом обнаружении симптомов инфекции сразу обращаться к врачу.
Хеликобактер от матери к ребенку передается не через плаценту, как иногда думают беременные женщины, а лишь воздушно-капельным путем. Поэтому необходимо избегать маме с инфекцией пробовать пищу и кормить ребенка одной и той же ложкой.
При такой инфекции проводится медикаментозная терапия антибиотиками. Помните, что препарат должен назначать только лечащий врач, он же контролирует процесс эрадикации болезнетворного микроорганизма. Не забывайте о сбалансированном питании и не игнорируйте прохождение повторного дыхательного теста.